mrna-1273 (spikevax®)和二价加强疫苗(缓冲液为 20mm tris,87mg/ml 蔗糖,10.7mm 醋酸钠,ph7.5)在-50℃至-15℃的冷冻存贮保质期为 9 个月,一旦解冻后,不允许再次冻存,在 2℃-8℃条件下可保存 30 天或者在 8℃-25℃条件下只能保存 24h;bnt162b2 (comirnaty®) 冷冻存贮甚至需要在-90 °c 至-60 °c 条件下,可保持 12 个月的稳定性。对于其儿科配方和二价加强新冠疫苗,辉瑞公司将缓冲液从含有 10%蔗糖的磷酸盐缓冲盐水(pbs)换成了含有 10%蔗糖的 tris(10mm)缓冲液,由于这种调整,使得新冠 mrna 疫苗在 2℃-8℃下的保质期可以从 1 个月增加到 10 周,而在-60℃至-90℃的长期储存可以保证长达 12 个月;相比之下,其他种类的新冠疫苗要显得皮实很多,在冷藏温度(2℃-8℃)下可存贮很长时间,例如,vaxzevria®(阿斯利康/牛津大学的腺病毒载体疫苗)可存贮 6 个月,nuvaxovid®(诺华的蛋白质疫苗)可存贮 9 个月,jcovden®(杨森的腺病毒载体疫苗)可存贮 11 个月 。通过上面的数据,我们可以看到,辉瑞和 moderna 对于新冠 mrna 疫苗的存贮有着严苛的规定,这主要是由于稳定性差,容易降解,是 mrna 天生的软肋。目前,获批上市的两款新冠 mrna 疫苗采用脂质纳米颗粒(lnp)作为递送载体,将 spike-mrna 包封起来。lnp 由可电离脂质、dspc、胆固醇以及 peg-聚乙二醇构成,例如,辉瑞生产的 bnt162b2 采用 alc-0315 作为可电离脂质,moderna 生产的 mrna-1273 采用 sm-102 作为可电离脂质。即便有了 lnp 的保护,mrna 依然表现得非常娇贵。因此,新冠 mrna 疫苗需要冷链运输或者存贮,这给其在全球的流通分配带来一定程度的障碍,尤其一些基础设施建设非常差的低收入国家。如果看过三体的朋友,一定对三体人晒干脱水度过乱纪元的桥段记忆深刻。类似的,如果要提升 mrna-lnp 疫苗在较高温度下的存贮保质期,目前比较现实可行的亚博电竞网的解决方案就是将疫苗冻干,去除掉疫苗制剂中的水分,在脱水状态下,分子流动性急剧下降,降解反应会受到极大的延缓,从而使得疫苗的热稳定得以提升,延长保质期。真空冷冻干燥是制药行业广泛应用的干燥工艺,先将液态制剂冷冻,再进行干燥升华,从而去除掉水分。有研究已经证实冷冻过程和干燥过程会对脂质纳米颗粒产生压力,所以需要加入冻干剂(lyoprotectants)或者称为赋形剂开稳定和保护脂质体结果。人们提出了两种理论来解释冻干剂发挥作用的机制:水替换理论和玻璃化理论。水替换理论认为,在冻干过程中,糖类可以替代水分子通过氢键与磷脂(如脂质体)相互作用,从而保护脂质膜结构。另一方面,玻璃化理论提出,糖类可以冷冻浓缩,随后进行玻璃化,形成高粘度的玻璃基质,从而防止脂质膜的变化。mrna-lnp 冻干相关的研究也已经有一些研究,我们曾经也分享过两期内容:和,但是,对于影响 mrna-lnp 冻干工艺关键参数的研究还远远不够深入。2023 年 3 月 30 号,比利时根特大学 rein verbeke 在 journal of controlled release 发表文章:continuous freeze-drying of messenger rna lipid nanoparticles enables storage at higher temperatures,这项研究新颖的地方在于没有选择传统分批冻干技术,而是采用基于旋转冷冻的连续冻干技术对 mrna-lnp 进行冻干,干燥时间变得更短,更加有利于进行过程和产品质量控制。尤其值得关注的是,他们发现可电离脂质和 mrna 的质量比以及缓冲液类型会影响 mrna-lnp 冻干前后的理化特性(尺寸、电位、分散系数以及形态),转染效率以及高温存储稳定性。由此,他们还得到两个非常重要的结论:第一,可电离脂质与 mrna 的质量比足够高时(20:1)能够有效防止冻干过程中 mrna 从脂质纳米颗粒中泄漏出来;第二,tris 缓冲液增强冻干 mrna-lnp 在较高温度下(22℃或者 37℃)的存贮稳定性,使得 mrna-lnp 转染效率能够保持至少 12 周。
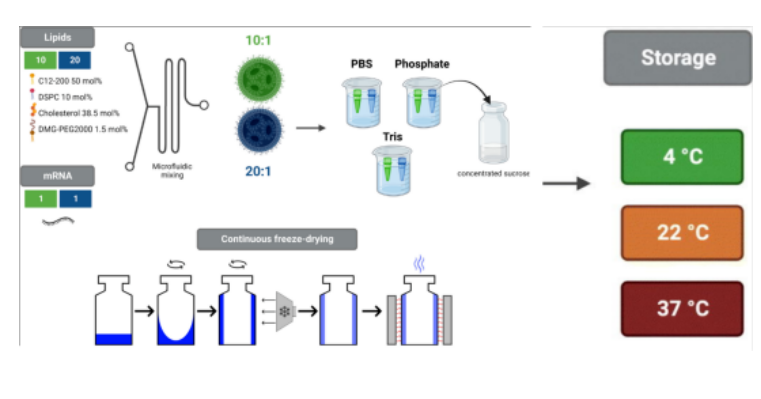
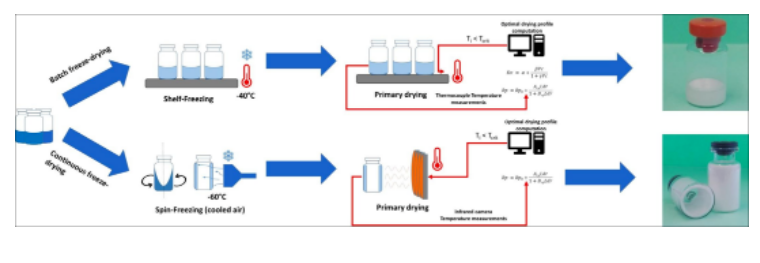
目前主流的冻干工艺仍然依赖传统的分批冻干(batch freeze-drying):在冻干过程中,装有液体制剂的小瓶需要放到冻干室的热控架(板层)上,通过板层的温度来实现冷冻过程和干燥过程。这种分批冻干工艺需要样品在架子上放置漫长的时间,大多数在 21 天到 7 天之间,严重限制产能。此外,装有液体制剂的小瓶之间在冻干室中位置的不同会影响冻干产品的关键质量属性(例如,残留水分,干饼结构等),这主要是由于热传导和成核时刻在整个板层上是不均匀的。如何理解传统的冷冻干燥工艺是批次干燥呢?打个比方,我往烤盘上放了十个鸡腿,将其放进烤箱架子上,关门烘烤。烘烤工艺是覆盖的是整个烤盘上的十个鸡腿,它的对象是一个整体批次,而不是架子上处于不同位置的某个鸡腿。所以说,一直到今天,单位剂量的冷冻干燥仍是作为一个批次进行的,在很大程度上,近一个世纪以来一直没有对这种批次冻干工艺做出改变。为解决单位剂量的冷冻干燥,有人开发了旋转冻干技术,它让装有液体制剂的小瓶沿其纵轴旋转,这样便可让小瓶内的液体均匀分布在瓶壁上面,随后使用冷气进行冻结。旋转冷冻后,小瓶会进入处于真空条件下的干燥室中,几个串联起来的红外热器在小瓶的连续入口处提供液体升华的能量,从而完成干燥过程。与传统的批量冻干相比,这种旋转冻干工艺也称为连续冻干技术(continuous freeze-drying),具有很多优点:第一,冻干时间大大缩短。旋转小瓶使溶液均匀地分布在小瓶内壁上,使得升华的表面积急剧增加,加速升华过程,提高干燥速度。第二,在一个连续干燥系统中,每一个小瓶都受到相同的工艺条件的影响。这意味着所有小瓶的传热都是相同的,而批量冻干系统则不然。第三,每个小瓶的关键工艺参数(cpp)和关键质量属性(cqa)可以在工艺过程中通过在线工艺传感器(如热成像、近红外)进行监测。打个比方说,连续冻干技术是针对每只鸡腿进行烘烤,能 100%控制产品质量,而传统的分批冻干则是对整个烤盘上的所有鸡腿进行烘烤,无法保证每只鸡腿烤出来的口味。
再来看看,可电离脂质与 mrna 的比例和缓冲液对于 mrna-lnp 冻干工艺的影响rein verbeke 等人选择的 lnp 配方为:c12-200(可电离脂质)、dspc、胆固醇以及 dmg-peg 2000 的摩尔比分为 50:10:38.5:1.5 mol%,包封甲基假尿嘧啶修饰-egfp-mrna。他们想知道 lnp 中更多的脂质和缓冲液中盐离子对于冻干过程的影响,因此,设定两个变量:第一,mrna:c12-200 质量比设定为 1:10 或者 1:20,第二,将缓冲液体系分别设为磷酸盐缓冲盐水(pbs)、磷酸盐缓冲液(pb)或 tris-缓冲液,ph 均为 7.4,缓冲能力为低(分别为 10、10 或 20mm)或者高(20、20 或 40mm),并补充了 12.5 m/v%的蔗糖作为冻干剂。然后,对于不同体系制备的 mrna-lnp 进行连续冻干处理,评估冻干后的理化特性和转染效率:所有体系的 lnp-mrna 配方,冻干前后的尺寸和 pdi 不存在显著差异。
当 c12-200:mrna 重量比为 10:1,mrna-lnp 冻干后:包封率和包封在 lnp 中的 mrna 量急剧下降,特别是对于 pbs 透析制备的 mrna-lnp 更为明显,包封率从 85%降低到只有 58%;zeta 电位也变得更负,增加缓冲能力无法防止 lmrna 泄漏和 zeta 电位的下降;采用 pbs 透析的,转染效率明显下降,而采磷酸盐和 tris 透析的,转染效率分别略有下降。
当 c12-200:mrna 重量比为 20:1,mrna-lnp 冻干后:mrna lnps 的包封率只有在使用 pbs 时才会降低(92%到 72%),而分散在磷酸盐和 tris 缓冲液中的 mrna-lnps 在冻干后包封率未发生改变;采用 pbs 透析的,转染效率明显下降,而采用 tris 和磷酸盐缓冲液的,转染效率保持不变。
总之,上述数据表明,当 c12-200 与 mrna 的质量比从 10 增加到 20,并且 pbs 被 tris 或磷酸盐缓冲液取代时,mrna-lnp在含有 12.5 m/v%蔗糖的制剂中可成功冻干,冻干过程不影响理化特性和转染效率。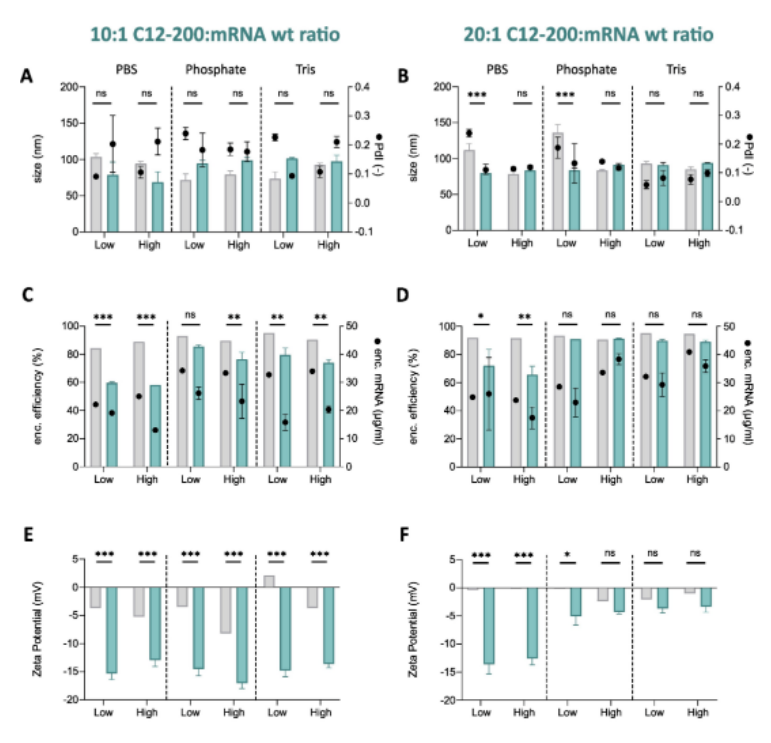
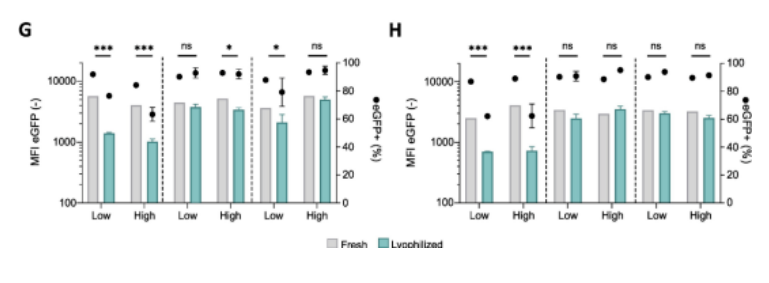
不同缓冲体系制备的 mrna-lnp 冻干前后的形态会发生怎样的变化呢?冷冻电镜显示透析缓冲液和冷冻干燥过程对 mrna-lnp 形态均会产生影响。采用 tris 中透析制备的 mrna-lnps 由固体无定形核心组成。有趣的是,在 pbs 中透析制备的 mrna lnps 表现出异质的形态,包括含有水泡结构的 lnps(内含 mrna)。此外,其中一些水泡结构与 lnp 完全分离,形成脂质体结构。一些悬浮在 tris 中的 lnps 在冻干后产生了水泡,这很可能是物理压力引起的相分离导致的。相反,悬浮在 pbs 中的 mrna-lnp 冻干后产生了多层结构,并且其中大部分没有水泡结构。
那么,冻干处理的 mrna-lnp 在不同存放条件下的稳定性是怎么样的呢?将 c12-200:mrna 质量比设为 20:1,用 ph 值为 7.4 的 tris 或磷酸盐缓冲液(低缓冲体系,tris 20 mm 和磷酸盐 10 mm)进行透析制备 mrna-lnp,并加入 12.5 m/v%的蔗糖作为冻干保护剂。测定冻干前后的 mrna-lnp 在 4℃存贮不同时间的理化特性和转染效率:此外,研究人员还将上述冻干前后 mrna-lnp(采用 20 mm tris 透析)放置在更高的温度(22℃或者 37℃)存贮,结果显示:相对液体的 mrna-lnp,冻干处理的 mrna-lnp 储存 12 周后转染效率并未发生显著变化;无论是液体或者是冻干 mrna-lnp 包封效率随着存贮时间延长均会发生轻微下降;冻干 mrna-lnp 在 37℃下储存 12 周时,颗粒大小从 80nm 增加到 150nm。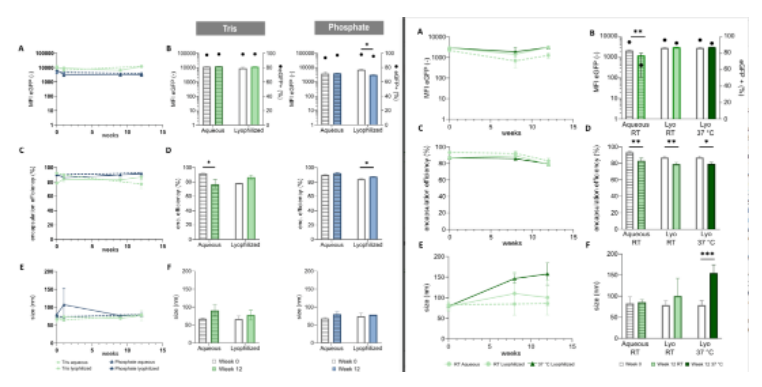
最后,研究者还证实冻干处理不会影响 fluc-mrna-lnp(c12-200:mrna 质量比设为 20:1, 20 mmtris 缓冲液)在小鼠体内的表达。
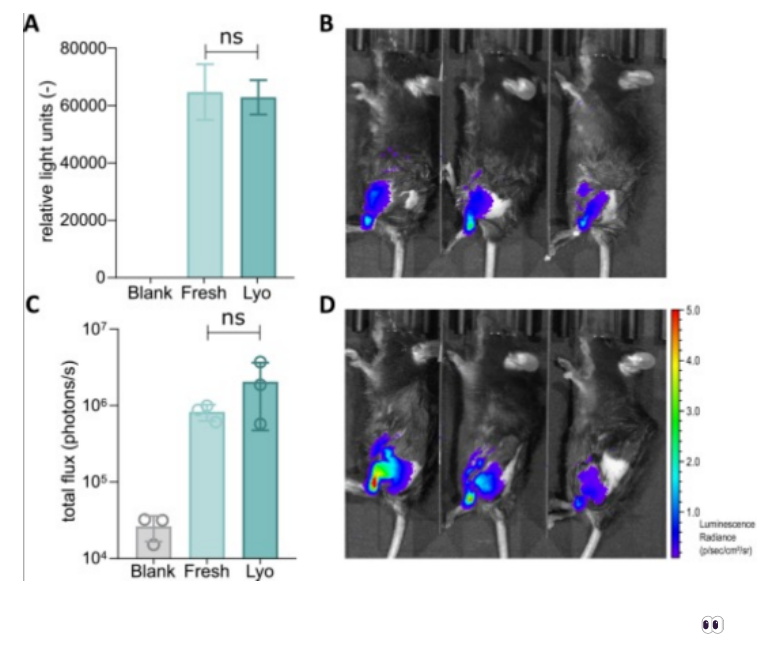
本期内容,我们讨论了分批冻干工艺和连续冻干工艺之间的区别,由此引出 mrna-lnp 连续冻工艺的相关研究。rein verbeke 发现 mrna 与可电离脂质的质量比、缓冲液类型会影响 mrna-lnp 冻干后的理化特性和转染效率,最终发现 c12-200:mrna 质量比为 20:1、选择 tris 缓冲体系制备 mrna-lnp 冻干效果最优,而且,相比液体制剂,冻干处理更加有利于在更高温度(22℃或者 37℃)下长时间存贮。但是,rein verbeke 等人制备的冻干 mrna-lnp 在22℃或者 37℃存贮时,相比 4℃,脂质纳米颗粒尺寸明显随着存贮时间的延长而增加,并且从存贮第一周时脂质纳米颗粒尺寸就已经出现明显的增加趋势。此外,rein verbeke 只是证实冻干工艺不会影响 mrna-lnp 体内的表达,对于高温下存贮不同时间点的冻干 mrna-lnp 在体内的表达效果并未做出检测。从目前的一些研究可以看出,新冠 mrna 疫苗的冻干处理是完全可行的,未来还需要对影响冻干工艺的因素做出进一步的研究,开发出在高温下长久存贮而不丧失活性的优化制剂配方和冻干工艺参数。






